A glikokalix emésztett egyedi rákos sejtek adhéziós eloszlása nagy térbeli felbontású jelölésmentes bioszenzor segítségével
Nanobioszenzorika Laboratórium
("Lendület" Kutatócsoport)
2022. június
A glikokalix a legtöbb sejttípus sejtfelszíni cukorrétege, amely nagymértékben befolyásolja a sejtek kölcsönhatását környezetükkel. Összetevői a glikolipidek, glikoproteinek és oligoszacharidok. Érdekes módon a rákos sejtek vastagabb glikokalix réteggel rendelkeznek, mint az egészséges sejtekben, de a mai napig nem született konszenzus a szakirodalomban a sejtfelszíni poliszacharidok és származékaik pontos szerepéről a sejtadhézióban és jelátvitelben. Korábbi munkánk során felfedeztük, hogy a rákos sejtek specifikus glikokalix komponensei szabályozzák az adhézió kinetikáját és erősségét RGD (arginin-glicin-aszparaginsav) peptiddel bevont felületeken. A kondroitináz ABC (ChrABC) enzimet használtuk a kondroitin-4-szulfát, kondroitin-6-szulfát és dermatán-szulfát komponensek emésztésére a rákos sejtek glikokalixában. Jelen munkánkban (Nicolett Kanyo, Kinga Dóra Kovács, Sándor Viktor Kovács, Bálint Béres, Beatrix Péter, Inna Székács, Robert Horvath. Single-cell adhesivity distribution of glycocalyx digested cancer cells from high spatial resolution label-free biosensor measurement. Matrix Biology Plus, 2022) egy nagy térbeli felbontású jelölésmentes optikai bioszenzort alkalmaztunk a rákos sejtek adhéziójának monitorozására mind egyedi sejt, mind populáció szinten. Az egyedi sejt adhézió populációs szintű eloszlását először rögzítettük ChrABC kezelés mellett. Elemeztük az adhéziós eloszlásban az enzimkezelés hatására bekövetkezett változásokat, és kiemeltük az enzimkezelés által leginkább érintett szubpopulációkat. A bemutatott eredmények új irányokat nyitnak a glikokalixszal kapcsolatos sejtadhéziós kutatások és az adhéziót befolyásoló célzottabb rákkezelések kidolgozásában.
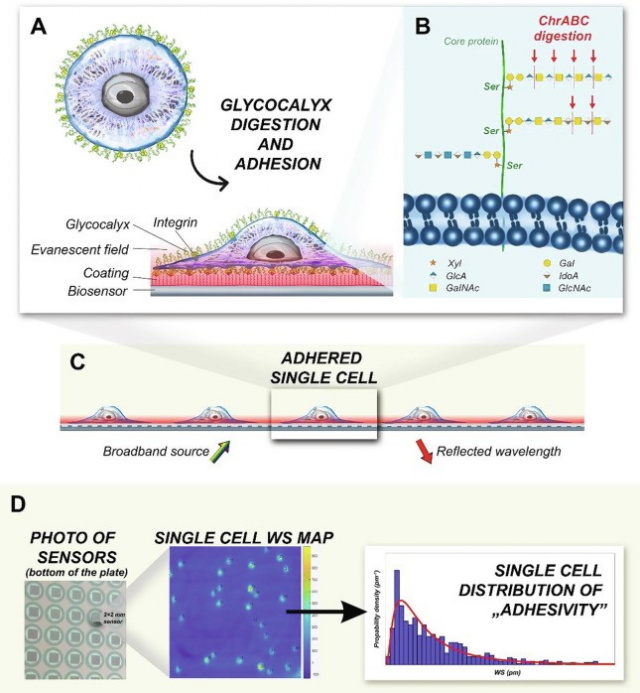
Az alkalmazott jelölésmentes módszer sematikus ábrázolása. A. ChrABC enzim leemészti a HeLa sejtek glikokalixának komponenseit. Az evanszcens tér (vörös árnyékterület) segítségével a PPR bevonatú bioszenzor felületén az emésztett sejtek adhéziós folyamata jelölésmentesen, valós idejű módon követhető nyomon. B. A glikokalix komponensek sematikus illusztrációja. A ChrABC lehasítja a dermatán-szulfátot, a kondroitin-4-szulfátot és a kondroitin-6-szulfátot. Lebontja az (1–4)-β-D-hexózaminil- és (1–3)-β-D-glukuronozil- (vagy (1–3)-α-L-iduronozil) kötéseket tartalmazó poliszacharidokat 4-dezoxi-β-t tartalmazó diszacharidokká. A sejtek az alulról megvilágított szenzorfelülethez tapadnak (szivárvány színű nyíl), és csak egy bizonyos rezonancia hullámhossz (piros nyíl) verődik vissza. Az evanszcens tér (vörös terület) a sejt-szubsztrátum érintkezési felületén belül hatol be a sejt felszíni struktúráiba. C. Az RWG bioszenzorral az egyedi sejtek is nagy felbontással vizsgálhatók. D. A berendezés 384 lyukú mikrolemezekkel működik, amelyek mindegyikében 2×2 mm-es RWG bioszenzorok találhatók (balra). Az eszköz elsődleges eredménye a hullámhossz-eltolódás (WS) térképe minden egyes lyukban (középen). Az egyes sejtek könnyen azonosíthatók, és tovább elemezhető a sejtadhézió populáció szintű eloszlása (jobbra).





