2024. májusi hónap kiemelt publikációi
Structural insights into the semiquinone form of human Cytochrome P450 reductase by DEER distance measurements between a native flavin and a spin labelled non-canonical amino acid
A humán Citokróm P450 reduktáz enzim szerkezetének és funkciójának vizsgálata a natív szemikinon gyök és a spinjelölt nemtermészetes aminosav közötti DEER spektroszkópiás távolságméréssel
Chemistry A European Journal, 2024
Maxime Bizet1, Deborah Byrne2, Frédéric Biaso1, Guillaume Gerbaud1, Emilien Etienne1, Giuseppina Briola1, Bruno Guigliarelli1, Philippe Urban3, Pierre Dorlet1, Tamas Kalai4, Gilles Truan3, Marlène Martinho1
1Aix Marseille Univ, CNRS, Bioénergétique et Ingénierie des Protéines, Marseille, France
2Protein Expression Facility, Aix Marseille Univ, Marseille, France
3TBI, Université de Toulouse, CNRS, Toulouse, France
4Department of Organic and Medicinal Chemistry, Faculty of Pharmacy, University of Pécs, Hungary
Szakmai összefoglaló
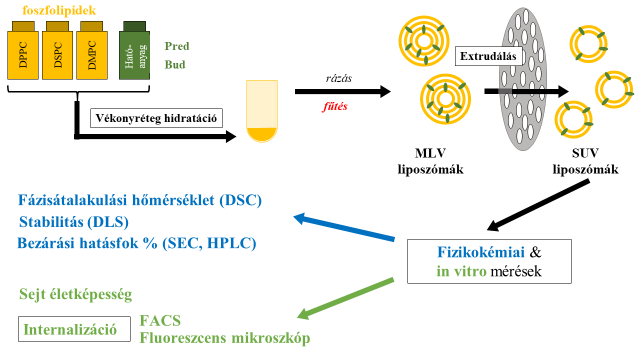
Francia kutatókkal együttműködve, oldatban lévő humán Citokróm P450 reduktáz enzim NaCl koncentráció változására bekövetkező konformárciós változásait vizsgáltuk nyitott/zárt állapotokat feltételezve. Ezt a PTE-n előállított ciklooktin alapú azidospecifikus spinjelző vegyülettel módosított azidofenilalanin oldallánc és a fehérje flavin csoportjából képzett szemikinon gyök távolságának DEER spektroszkópiával történő meghatározásával értük el. Ezen konformációs változásoknak jelentős hatása van a NADPH és a Citokróm P450 közötti elektronátmentekre.
Közérthető ismertető
Francia kutatókkal együttműködve a PTE kutatói a Citokróm P450 reduktáz szerkezetének és funkciójának tanulmányozására a molekula szerkezeti sajátságait kihasználva és a fehérje szerkezetét szelektíven módosítva kaptunk információkat. A stabilis szabad gyökökkel módosított fehérjét DEER-spektroszkópiával („molekuláris vonalzó”) vizsgálva szereztünk információkat a fehérje alakjának (konformációjának) működés közbeni megváltozásáról.
Cyclodextrin encapsulation enabling the anticancer repositioning of disulfiram: Preparation, analytical and in vitro biological characterization of the inclusion complexes
Ciklodextrin kapszulázás, amely lehetővé teszi a diszulfirám rákellenes újra pozicionálását: A zárványkomplexek előállítása, analitikai és in vitro biológiai jellemzése
International Journal of Pharmaceutics, 2024
Beáta-Mária Benkő1, Gergő Tóth2, Dorottya Moldvai3, Szabina Kádár2,4, Edina Szabó4, Zoltán-István Szabó5, Márta Kraszni2, Lajos Szente6, Béla Fiser7,9, Anna Sebestyén3, Romána Zelkó1, István Sebe1,10
1University Pharmacy Department of Pharmacy Administration, Semmelweis University, Budapest, Hungary
2Department of Pharmaceutical Chemistry, Semmelweis University, Budapest, Hungary
3Tumor Biology, Cell and Tissue Culture Laboratory, 1st Department of Pathology and Experimental Cancer Research, Semmelweis University, Budapest, Hungary
4Department of Organic Chemistry and Technology, Faculty of Chemical Technology and Biotechnology, Budapest University of Technology and Economics, Műegyetem rkp. 3., Budapest 1111, Hungary
5Faculty of Pharmacy Department of Drugs Industry and Pharmaceutical Management, George Emil Palade University of Medicine, Pharmacy, Science and Technology of Targu Mures, Romania
6CycloLab Cyclodextrin Research & Development Laboratory Ltd., Budapest, Hungary
7Institute of Chemistry, Faculty of Materials Science and Chemical Engineering, University of Miskolc, Hungary
8Department of Physical Chemistry, Faculty of Chemistry, University of Lodz, , Poland
9Ferenc Rakoczi II Transcarpathian Hungarian College of Higher Education, Beregszász, Transcarpathia, Ukraine
10Egis Pharmaceuticals Plc., R&D Directorate, Budapest, Hungary
Szakmai összefoglaló
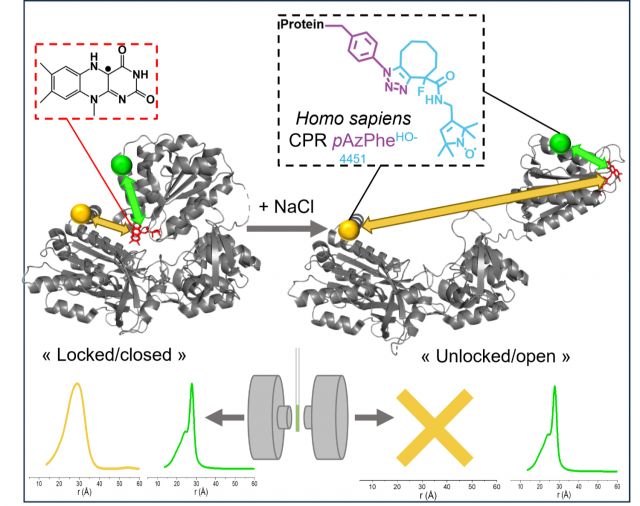
A gyógyszerek újra pozícionálása kulcsfontosságú a rákkutatásban a tartósan fennálló, kielégítetlen igények megoldására. A rákterápiában ígéretes diszulfiram alacsony biohasznosíthatóságú. A ciklodextrinekkel történő molekuláris kapszulázása növeli az oldhatóságát és stabilitását, 1000-szeres oldhatóságnövekedést és egyperces gyors kioldódást mutat. A rákos sejteken végzett kísérletek azt mutatják, hogy eltérő mértékben, de hatásos a nehezen kezelhető tumorok, melanoma és a glioblasztóma ellen.
Közérthető ismertető
A rákos sejteken végzett kísérletek kimutatták, hogy a ciklodextrin-kapszulázás hatékonyan fokozza a diszulfirám terápiás hatását, mivel jelentősen megnöveli az oldhatóságát és stabilitását, különösen a melanoma és az idegrendszer legrosszindulatúbb tumoros elváltozása, a glioblasztóma esetében.
Long-term shelf-life liposomes for delivery of prednisolone and budesonide
Prednizolon és budezonid tartalmú liposzómás gyógyszerhordozó rendszerek fejlesztése
Journal of Molecular Liquids, 2024
Bálint Budavári1, Áron Karancsi1, Balázs Gábor Pinke2, Éva Pállinger3, Krisztina Juriga-Tóth1, Márton Király4, Zsófia Szász3, István Voszka5, Kolos Molnár2,6.7, László Kőhidai, Angéla Jedlovszky-Hajdú, Krisztina S. Nagy1
1Laboratory of Nanochemistry, Department of Biophysics and Radiation Biology, Semmelweis University, Budapest, Hungary
2Department of Polymer Engineering, Faculty of Mechanical Engineering, Budapest University of Technology and Economics, Hungary
3Department of Genetics, Cell- and Immunobiology, Faculty of Medicine, Semmelweis University, udapest, Hungary
4Department of Pharmaceutics, Faculty of Pharmacy, Semmelweis University, Budapest, Hungary
5Department of Biophysics and Radiation Biology, Faculty of Medicine, Semmelweis University, Budapest, Hungary
6ELKH–BME Research Group for Composite Science and Technology, Budapest, Hungary
7MTA-BME Lendület Sustainable Polymers Research Group, Budapest, Hungary
Szakmai összefoglaló
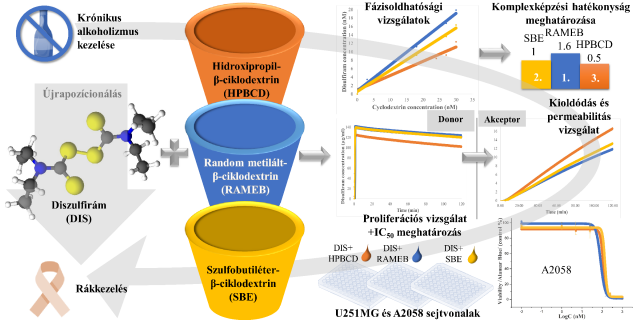
Jelen kutatás tárgya olyan liposzómás gyógyszerhordozó rendszerek létrehozása volt, amelyek megfelelnek a jövőbeli gyógyszerjelöltek alapvető fizikai-kémiai és biológiai kritériumainak: kellő mértékben megőrzik stabilitásukat hosszútávon, kimagaslóan nagy hatóanyag-bezárási hatásfokkal rendelkeznek, a sejtek életképességét nem befolyásolják negatív módon, valamint bizonyíthatóan bejutnak a sejtbe. A következő célunk, hogy inhalációs úton tudjuk alkalmazni ezeket például asztma-terápiában.
Közérthető ismertető
Ebben a kutatásban olyan gyógyszerhordozó rendszert hoztunk létre, amely alkalmas lehet arra, hogy sikeresen juttassa célba a bezárt gyulladáscsökkentő hatóanyagot. Ezen felül kiemelkedően hosszú stabilitással rendelkezik, és a sejtekre életképességére sem hat negatívan. A jövőben azt szeretnénk elérni, hogy inhalációs úton alkalmazhatóvá tegyük ezt a gyógyszer-jelöltet, például asztma terápiában.