Magyar térszerkezet-kutatók tárták fel az „egészséges” amiloidok molekuláris működését
Ha manapság az amiloidokról esik szó, legtöbbünknek a neurodegeneratív betegségek, főként az Alzheimer- és Parkinson-kór jut eszébe, hiszen e betegségeket a legelfogadottabb elméletek szerint a kóros amiloidok lerakódása és felhalmozódása okozza az idegsejtekben. Perczel András akadémikus, az ELTE egyetemi tanára és kutatócsoportja azonban az általuk használt világszínvonalú molekuláris képalkotó eszközök segítségével feltárta, hogy a vércukorszint szabályozását befolyásoló egyes hormonok miként képesek váltogatni térszerkezetüket a funkcionális amiloid- és a bioaktív formájuk között.
Mi is az az amiloid? Bár azt gondolhatjuk, hogy egy konkrét betegséget okozó fehérje neve, hiszen az Alzheimer-kór kapcsán nap mint nap szerepel a tudományos hírekben, valójában
a peptidek és fehérjék egy olyan térszerkezeti formájáról van szó, amelyet szabályos rend és tömör szerkezeti rétegződés jellemez.
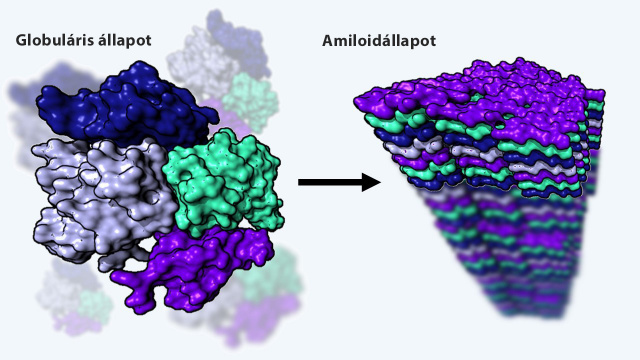
Perczel András hasonlatával élve ezt a „katonás rendet” jellegzetes és ismétlődő molekuláris kölcsönhatások biztosítják az akkurátusan felsorakozó poliamidszálak között. Az amiloidok térszerkezeti felépítése a közös vonások mellett számos egyedi tulajdonsággal bír, megjelenik például a polimorfizmus jelensége, miszerint egyazon aminosavsorrend mellett többfajta amiloidforma állítható elő, ahogy ezt az ő munkájuk is bizonyítja. Bár egyes betegségek kapcsán patológiás amiloidstruktúra figyelhető meg, nem minden amiloid okoz betegséget, mi több, létfontosságú élettani funkciójuk is lehet.
 Perczel András Fotó: mta.hu
Perczel András Fotó: mta.hu Az amiloidok a neurodegeneratív betegségek népegészségügyi gondjai miatt kerülnek újra és újra a közélet és a tudományos kutatás fókuszába: valóban nagy baj okozói! Az amerikai orvostudományi alapkutatásokat finanszírozó Nemzeti Egészségügyi Intézet (NIH) előrejelzése szerint a társadalom öregedésével és az Alzheimer-, illetve Parkinson-kór terjedésével hamarosan már több százmilliárd dollárban lesz mérhető a neurodegeneratív betegségek kezelésére, illetve a betegek ellátására fordított egészségügyi költségek mértéke csak az Egyesült Államokban. És ez nem a terápiás költség, hiszen a neurodegeneratív betegségek progressziója a világszerte folyó intenzív kutatások dacára mindmáig nem fordítható meg. Érdemes megjegyezni azért, hogy vannak ígéretes hatóanyagjelöltek (pl. lecanemab) a betegség előrehaladásának lassítására.
Hatalmas jelentősége van tehát az amiloidstruktúrák működésének hátterében sejtett szerkezeti és biokémiai folyamatok közötti kapcsolat feltérképezésének.
Az ELTE Szerkezeti Kémia és Biológia Laboratóriumában, amelyet molekuláris képalkotó eszközparkja révén a hazai top50 kutatási infrastruktúrák közé is beválasztottak, régóta kutatják az amiloidok szerepét és működését. Legújabb felfedezéseiket most közölte a Nature lapcsaládhoz tartozó Nature Communications folyóirat.
„A mi korábbi kutatásaink is azt bizonyítják, hogy a neurodegeneratív betegségeket okozó amiloidok az öregedéssel és a genetikai betegségekkel összefüggő fehérje-homeosztázis meghibásodásának szomorú melléktermékei – mondja Perczel András. – De azt is látnunk kell, hogy amiloidképződés társul egy sor egészséges élettani funkcióhoz is. Ma már tudjuk, hogy az amiloidok jótékony hatása például a gerincesek megjelenése óta bizonyosan jelen van az élőlényekben, s hatékonyan segítik egyes fehérjék tárolását.”
Perczel András és kollégái feltárták, hogy
az amiloidstruktúrák egyik jótékony hatása az emberi szervezetekben a hormonok termeléséhez, tárolásához, majd felszabadításához kapcsolódik.
Kutatásaik révén bizonyították, hogy a vércukorszintet szabályozó peptidhormonok (amelyekre időszakosan, jellemzően az étkezések kapcsán, a vércukorszint egyenletes szinten tartása érdekében van szükség – de akkor hirtelen és nagy mennyiségben) a létrejöttüket követően amiloidrostokká állnak össze. Ezzel a technikával, szeparáltan kis helyen sok peptidmolekulát lehet időszakosan stabil formában tárolni. Ezek a hormonamiloidok savas vezikulákba, kis membránnal borított hólyagokba csomagolva várják a jelzést, hogy a véráramba jussanak, és ott ellássák szabályozó tevékenységüket. A vér semleges pH-ja pillanatszerűen felbontja az amiloid-téralkatot, gyorsan visszaalakulnak a különálló, funkcionális térszerkezetű, biológiailag aktív formába, és másodpercek alatt kifejthetik szabályozófunkciójukat a megfelelő receptorokon. Vagyis ebben az esetben az amiloidszerkezet biztosítja a hatékony tárolás és a gyors felszabadítás együttes képességét, amelyhez hasonló más hatékony mechanizmus nem ismert.
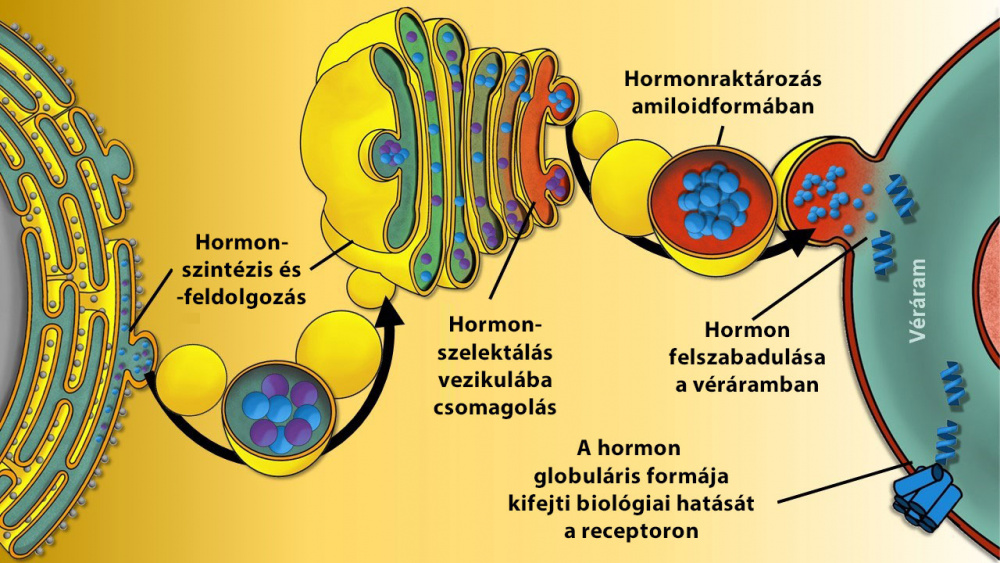 Hormonfehérjék szintézise, feldolgozása, raktározása „jótékony” vagy funkcionális amiloidformában, végül az amiloidrostok szétesését követően a célreceptorhoz való juttatásuk
Hormonfehérjék szintézise, feldolgozása, raktározása „jótékony” vagy funkcionális amiloidformában, végül az amiloidrostok szétesését követően a célreceptorhoz való juttatásuk„Ezt a hormontárolási formát úgy kell elképzelnünk, mint a konzervet. A sejtek előre legyártanak nagy mennyiségű hormont, amit »konyhakész« állapotban elraktároznak – folytatja az akadémikus. – A kérdésünk az volt, hogy e célra miért különösen alkalmas az amiloidstruktúra, és milyen módon zajlik az oda- és visszaalakítás atomi szinten. Azt tudtuk, hogy a hormonokat nem lehet a bioaktív alakjukban tárolni, mert a hormonszabályozást végző bontó enzimek gyorsan lebontanák őket. Nagyon fontos az a felismerésünk, hogy a létrejövő amiloidok savas vezikulákba kerülve stabilak, de semleges körülmények közepette labilisak, s ezért esnek szét szálakra. Ezt a képességet a hormonszekvenciában található savas aminosavak (aszparaginsav és glutaminsav) mint molekuláris kapcsolók hordozzák. Ezek az aminosavak biztosítják a hormonok azon képességét, hogy eltérő kémhatású közegben eltérő önszerveződő képességgel rendelkeznek: ha kell, akkor »individuumok«, ha kell, akkor »jól szervezett közösséget« alkotnak.”
A mostani felfedezés a hormonok amiloiddá, majd visszaalakulását szabályzó aminosavak szerepére, a térszerkezet-szabályzó funkciójukra fókuszál.
Horváth Dániel – az egyik fiatal kutató – rámutatott arra, hogy ezek a kapcsolók és szekvenciális környezetük evolúciósan nagymértékben konzerváltak, vagyis szinte semmit sem változtak a sok százmillió év evolúciója során. A kémhatástól függő szabályos nanostruktúrák kialakulásának (amiloidképzés) és felbomlásának megértése túlmutat a hormonok egészséges működésének megértésén, s elvezet a nano- és mezostruktúrák racionális tervezéséhez, amelyekben e peptidhormon-asszociátumok alkalmasak lehetnek hatóanyag-hordozó rendszerek kifejlesztésére.
 A kutatócsoport munkatársa, Dürvanger Zsolt által röntgenkrisztallográfiai módszerek segítségével meghatározott hormon amiloid téralkatainak sematikus rajzolata
A kutatócsoport munkatársa, Dürvanger Zsolt által röntgenkrisztallográfiai módszerek segítségével meghatározott hormon amiloid téralkatainak sematikus rajzolataMindezek a felfedezések nem történhettek volna meg,
ha a kutatócsoport nem dolgozna a térszerkezet-kutatás három legfontosabb képalkotó eljárásával, a röntgendiffrakcióval, az NMR (magmágneses rezonancián alapuló) spektroszkópiával, illetve a krio-elektronmikroszkóppal.
„Képesek vagyunk egyszerre nagy és kis felbontású spektroszkópiai vizsgálatokat is végezni, melyek akár egyes emlősenzimek atomjainak belső mozgékonyságáról is rögzíthetnek pillanatképeket. Fél évvel ezelőtt e térszerkezet-vizsgálatok révén kétszer is a Chemical Science folyóirat címlapjára kerültünk, vagyis az eredményeink alkalmasint tényleg világszínvonalúak – érvel Perczel András. – Az általunk alkalmazott módszerek kiegészítik egymást, mert valójában a röntgendiffrakció, az NMR és a krio-elektronmikroszkópia együttes alkalmazása tud kellő pontosságú képegyüttest adni a legkülönbözőbb szerkezeti és biokémiai problémák megértéséhez. Bár e kutatási infrastruktúra fenntartása és működtetése egyszerre igényel komoly pénzügyi forrásokat és szakértelmet, ahhoz, hogy a magyar szerkezeti kémia és molekuláris biológia továbbra is világszínvonalú sikereket érhessen el, a megléte és fenntartása elengedhetetlen.”
Az osztályelnök akadémikus szerint a kutatási eszközök mellett az MTA biztosította anyagi és szellemi támogatás is kell az ilyen felfedezésekhez. „E kutatások szellemi hátterét az Akadémia biztosítja.
A részt vevő kutatócsoportok ezer szállal kötődnek az MTA-hoz, a kutatásaink pedig szervesen illeszkednek az Akadémia által felvállalt, hatalmas nemzeti tudományos jelentőséggel bíró kutatóprogramokba.
A Magyar Tudományos Akadémia nemcsak a magyar tudományosság legmagasabb szintjein folyó kommunikációban játszik pótolhatatlan szerepet, de a felfedezéseket is hitelesen és megbízhatóan közvetíti a nyilvánosság felé. Ez éppen az ilyen, jelenleg még gyógyíthatatlan betegségek elleni küzdelemhez szorosan kapcsolódó felfedező kutatások esetében pótolhatatlan.”
Az MTA Kémiai Tudományok Osztálya havi rendszerességgel mutatja be közérthető formában a kémiai szakterületet és határterületeit érintő friss és kiemelkedő jelentőségű, már publikált közleményeket "A hónap publikációja" címmel. 2023. augusztus hónap egyik kiemelt publikációja Perczel Andrásnak és kollegáinak a Nature Communicationsban megjelent cikke lett.




