Az immunrendszer svájci bicskája: újabb akadémiai sikersztori Szegedről
Egy fiatal orvos-kutató, Manczinger Máté tisztán bioinformatikai eszközökkel fedezte fel az emberi immunrendszer és a kórokozók sokfélesége közötti alapvető összefüggést. Az MTA Szegedi Biológiai Kutatóközpontban, Pál Csaba világszínvonalú műhelyében végzett munka eredményei a védőoltások alkalmazásában és az antibiotikumos kezelés megválasztásában is fontosak lehetnek.
Az egyre gyarapodó biológiai adatbázisok publikus elérhetősége soha nem látott esélyhez juttatja a magyar kutatókat. Az amerikai szövetségi és európai uniós kutatásfinanszírozó szervezetek ahhoz a feltételhez kötik támogatásukat, hogy a kutatás során létrejött adatok nyilvánosan hozzáférhetők legyenek. Így áll elő az a számunkra (is) kedvező helyzet, hogy a „mások pénzén” megtermelt irdatlan adattengerben szinte ingyen lubickolhatunk: nem kell hozzá más, mint egy internetkapcsolattal rendelkező számítógép. Meg persze – és itt rejlik a lényeg – kell egy ötlet, hogy mit és miért keressünk.
 Manczinger Máté Forrás: saját felvétel
Manczinger Máté Forrás: saját felvételManczinger Máté ötlete – amint azt a vele és mentorával, az MTA SZBK Evolúciós Rendszerbiológiai Csoportot vezető Pál Csabával folytatott beszélgetésből megtudtuk – úgy indult, mint körvonalazódó feltevés a kórokozóknak az immunrendszerre (pontosabban az MHC-immunfehérjék evolúciójára) gyakorolt hatásáról. A fiatal orvos-kutató elméletének lényege az volt, hogy
ha sok kórokozó van a környezetben, akkor ennek hatására az immunrendszer is sokoldalúbbá válik.
Ezt az állapotot azonban nem érdemes általában fenntartani, valószínűleg azért, mert kevésbé hatékony egy-egy kórokozó ellen, és nagyon költséges a szervezet számára.
Egy hasonlattal élve: a sok kórokozót tartalmazó területeken elengedhetetlen lehet a túléléshez a svájcibicska-szerű sokoldalúság. Ha elveszünk a dzsungelben, és egyetlen eszközzel kell boldogulnunk, jó, ha az a szerszám kés, villa, olló, csavarhúzó és iránytű is egyben. De ha nem épp ezer veszély leselkedik ránk, praktikusabb mindig az adott feladatra legalkalmasabb eszközt választanunk, és a maguk szakterületén semmilyen svájci bicska nem vetekedhet a kenyérvágó késsel, a körömollóval vagy a motoros csavarbehajtóval.
Egy kíváncsi orvos esete a bioinformatikával
Manczinger Mátét, aki a Szegedi Tudományegyetemen szerzett diplomája után bőrgyógyászként szakvizsgázott, a megoldatlan problémák iránti vonzódása terelte a kutatás felé, és gyakorló orvosi munkája mellett önállóan kezdte bioinformatikai ismereteit gyarapítani. Hamar rájött, hogy hipotézisének ellenőrzéséhez minden adat „ott van kinn” a világhálón, csak több független adatbázisban szétszórva, s ezeket az adatokat még senkinek sem jutott eszébe összefésülni.
Formálódó feltételezésével először a Bőrgyógyászati Klinika igazgató professzorát, Kemény Lajost kereste meg, és együtt vették fel a kapcsolatot Pál Csabával és Papp Balázzsal. A 2015-ben Bolyai-díjjal kitüntetett, évek óta a legrangosabb folyóiratokban publikáló laborvezető örömmel vállalta Manczinger Máté mentorálását, noha a témafelvetés csak nagyon lazán illeszkedett a kutatócsoport fő csapásirányába, a bakteriális antibiotikum-rezisztencia evolúciójának kutatásába.
„A mentorálást kiemelten fontos tevékenységnek tartom – mondja Pál Csaba. – Ha egy fiatal kutató, legyen akár még csak BSc-s vagy már posztdoktor, megkeres egy jó gondolattal, ami legalább szegről-végről kapcsolható a profilunkhoz, nyitottak vagyunk rá.
Meg kell akadályoznunk, hogy fiatal tehetségek támogatás és lehetőség híján elvesszenek a hazai tudomány számára.”
A nagy lökést a Nemzeti Kutatási, Fejlesztési és Innovációs Hivatal (NKFIH) öt évre szóló, jelentős támogatási összegű Élvonal-pályázata adta, amelyet az MTA-kutatócsoport kimondottan erre a témára nyert el. Innentől fogva a projekt villámgyorsan haladt a végkifejlet felé: mindössze másfél év alatt összeállt egy olyan cikk anyaga, amely a rangos PLoS Biologyban jelent meg, és amelyben sikerült bizonyítékokkal alátámasztani az eredeti elképzelést.
 Pál Csaba (jobbra) és kutatótársai szegedi laboratóriumukban Forrás: mta.hu/Szigeti Tamás
Pál Csaba (jobbra) és kutatótársai szegedi laboratóriumukban Forrás: mta.hu/Szigeti TamásFőszerepben a fiatalok
„Fontos üzenet a diákoknak, hogy a bioinformatika segítségével három-négy év alatt simán össze lehet hozni egy PhD-fokozatot – mondja Manczinger. – Egy hasonló, erősen hipotézisvezérelt munkában az alapötlet után a kivitelezés már egyszerű: csak programozás és statisztika kell hozzá.”
A kutatásnak fontos eredményei lehetnek az orvostudomány számára is. A kutatócsoport most azon dolgozik, hogy összefüggést mutasson ki a védőoltások hatékonysága és az immunrendszer sokoldalúságának oka között.
A kutatók számára tehát a PLoS Biology-cikk inkább a kezdete, mint a lezárása egy olyan izgalmas új kutatási irányvonalnak, amelyben – Pál Csaba kutatócsoportjának hagyományos erősségeihez illeszkedve – a főszerepet a bioinformatika játssza, s amely ezért remélhetőleg nemcsak Mátét, de még több hasonló érdeklődésű fiatalt tarthat meg a hazai tudománynak. Ami Manczinger Mátét illeti, ő egyelőre nem vágyódik külföldre. „Személy szerint lokálpatrióta típus vagyok, és nincs bennem olyan hajtóerő, ami a távozásra kényszerítene – fejtette ki. – A bioinformatika eszközei itt is adottak, és nem látom, milyen előnnyel járna számomra, ha külföldön folytatnám ugyanezt.”
Pál Csaba már nem látja ennyire felhőtlennek a hazai helyzetet: attól tart, hogy az MTA-kutatóhálózat finanszírozása körüli bizonytalanságok azokat is elrettentik a maradástól vagy a hazatéréstől, akiknek ez volt az eredeti szándékuk. „Izraelben, Kanadában, San Franciscóban dolgoznak most olyan tehetséges tanítványaim, akiket visszavártam, de akiknek a hazatérése az itthonról érkező hírek miatt kétségessé vált. A helyzet mostani kiszámíthatatlansága két-három éven belül kézzelfogható munkaerőhiányt fog okozni – vizionálja a csoportvezető. – Ezért legalább azoknak, akik olyan szerencsés helyzetben vannak, mint én, és érdemleges pályázati forrásokkal rendelkeznek, segíteniük kell a hazai tehetségeket. Ezzel megalapozzuk a mentoráltak jövőjét, akiket eljuttatunk a legjobb külföldi laborokba, de remélhetjük, hogy utána visszatérnek. Izraelben például ez fantasztikusan működik: az MIT-re, a Harvardra, a Stanfordra küldik a fiatalokat, akikben megvan az igény, hogy hazatérjenek, és olyan tapasztalatot visznek haza, ami pénzben nem kifejezhető.”
A Szegedi Biológiai Kutatóközpont az MTA kutatóintézet-hálózatának egyik legjobb teljesítményű, legdinamikusabban fejlődő intézménye. Mint arról korábban beszámoltunk, Nagy Ferenc, a 2018 elején megválasztott új főigazgató új alapokra akarja helyezni a Biokémiai Intézetet, a kutatói kiválóság alapján építené tovább a közösséget, és a jó pénzügyi helyzetet is kihasználva tenné az intézményt hosszú távon is eredményessé.
Pál Csaba kutatócsoportjáról és két másik kiváló SZBK-s csoportról ebben a cikkünkben olvashat.
A svájci bicska anatómiája – a kutatás biológiai háttere
Az immunrendszer legfontosabb feladata, hogy a kórokozókat megkülönböztesse a saját sejtjeinktől. Ebben a folyamatban játszanak alapvető szerepet az MHC-molekulák azáltal, hogy megkötnek és bemutatnak ránk és a kórokozókra jellemző molekulákat az immunrendszer számára. Ez a lépés elengedhetetlen a fertőző betegségek túléléséhez és az autoimmun betegségek elkerüléséhez. Az MHC-molekulák nagy változatosságot mutatnak, ami miatt két ember nagy valószínűség szerint eltérő molekulákat hordoz. Egyes variánsok autoimmun betegségekre, mások különböző fertőző megbetegedésekre hajlamosítanak. A kutatók munkájuk során a molekulák olyan tulajdonságait vizsgálták, amelyek megmagyarázhatják azok összefüggéseit különböző betegségekkel, valamint hatással lehetnek az egyes variánsok földrajzi elterjedésére.
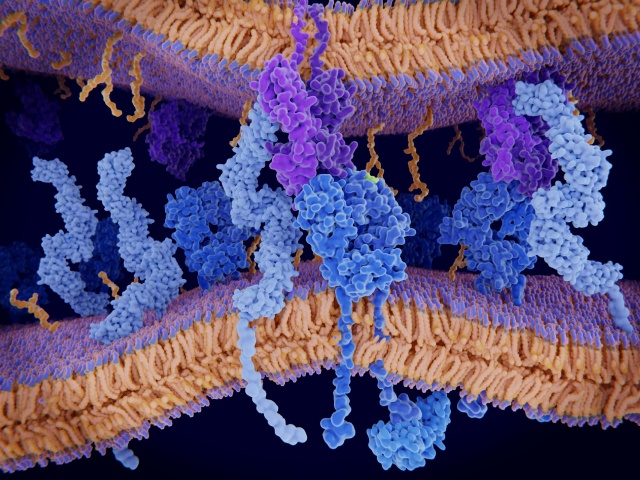 Egy T-sejt membránján elhelyezkedő MHC-molekula (lila) és az általa megkötött antigén (világoskék). A kép illusztráció Forrás: istockphoto.com
Egy T-sejt membránján elhelyezkedő MHC-molekula (lila) és az általa megkötött antigén (világoskék). A kép illusztráció Forrás: istockphoto.comNagyon egyszerű hipotézisből indultak ki. Az MHC-molekulák között vannak olyanok, amelyek kevés, míg mások nagyszámú eltérő molekulát képesek megkötni. Az előbbieket specialistáknak, míg utóbbiakat generalistáknak nevezzük. A kevesebb megkötött molekula kevesebb kórokozó felismerését teszi lehetővé, aminek komoly következménye lehet a fertőző betegségekkel vívott harcban.
A kutatók arra gondoltak, hogy a generalista MHC-molekulák olyan területeken – például a trópusokon – terjedtek el, ahol nagyszámú eltérő fertőző betegség van jelen. Mivel ezek a variánsok több kórokozó molekuláit képesek megkötni, több fertőző betegséggel szemben nyújtanak védelmet, mint specialista társaik. Ugyanakkor a specialista MHC-molekulák ott fordulnak elő, ahol a fertőző betegségek száma alacsony, például Észak-Európában. A világhálón elérhető feldolgozott adatbázisok alapján ez a trend még a vártnál is erősebb volt. Megállapítható, hogy valóban a kórokozók és az általuk okozott fertőzések száma határozza meg a specialista és generalista MHC-változatok elterjedését. Az eredmény alátámasztja a molekulák rendkívüli szerepét is a kórokozók és az ember közös evolúciójában: az emberi populációk Afrikából történő kivándorlása során újabb és újabb kórokozókkal találkoztak, és csak azok élhették túl a fertőző betegségeket, akik ellenállóbbak voltak velük szemben.
Fontos kérdés, hogy a generalista MHC-molekulák kizárólag előnyt jelentenek-e hordozóik számára. Ennek az ellenkezőjére utal, hogy azokon a területeken, ahol kevesebb kórokozó található, a specialisták terjedtek el. Valóban, a generalisták nemcsak a kórokozók, hanem saját sejtjeink molekuláiból is többet kötnek meg, ami hajlamosíthat autoimmun és allergiás megbetegedésekre. Emellett egy, a kórokozóra kifejezetten jellemző molekula felismerése bizonyos esetekben hatékonyabb immunválaszt eredményezhet.
A kutatók jelenleg az NKFIH Élvonal-pályázatának keretében azt szeretnék megválaszolni, hogy a generalista MHC-molekulákat hordozó emberek jobban reagálnak-e a védőoltásokra, illetve hajlamosabbak-e autoimmun és allergiás megbetegedésekre.
További információ
Manczinger Máté
matemanc@gmail.com




