Magyar kutatók eredménye is segíthet a szuperbaktériumok ellen
A DNS-ben keletkezett hibák javításának kutatása során egy új, ígéretes gyógyszercélpont merült fel a baktériumok elleni küzdelemben. Az antibiotikum-rezisztencia korunk egyik legsúlyosabb egészségügyi problémája. Az ELTE-MTA Lendület Motorenzimológiai Kutatócsoport cikke a PNAS-ben jelent meg.
Az élőlények számára létfontosságú a genom épségének fenntartása, ezért a DNS-ben folyamatosan bekövetkező hibák kijavítására hatékony és precízen szabályozott javítómechanizmusok alakultak ki.
Az elkerülhetetlen DNS-károsodások létfontosságú javítása azonban gyakran a kiinduló hibás állapotnál is veszélyesebb köztes termékeken keresztül zajlik. Az ilyen DNS-szerkezetek félresikerült feldolgozása az eredeti hibánál is súlyosabb bajt, például rákos átalakulást okozhat. A javítás helyes irányba terelésének, azaz „minőség-ellenőrzésének” mechanizmusai azonban jórészt ismeretlenek. A Kovács Mihály által vezetett ELTE-MTA Lendület Motorenzimológiai Kutatócsoport tagjai egy új, a különböző DNS-szerkezetek eltérő feldolgozásán alapuló minőség-ellenőrző folyamat felderítését publikálták a PNAS-ben. A munka eredményei egy ígéretes új kutatási irányt is megalapoznak.
Nem mindegy, hogyan sikerül: a DNS-javítás minőség-ellenőrzése
Ha a DNS mindkét szála eltörik, az a genom instabilitását, a sejt halálát, illetve magasabb rendű szervezetekben a sejt rákos átalakulását okozhatja. A minden élőlényben zajló, homológ rekombináció nevű folyamat a kettős DNS-száltöréseket – egy épen maradt DNS-kópia információtartalmának felhasználásával – potenciálisan hibamentesen tudja helyreállítani.
A homológ rekombináció kulcsszereplői közé tartozó, a baktériumokban és az emberben is megtalálható DNS-helikáz motorenzimek kémiai energia felhasználásával mozognak a DNS-molekula mentén, és szétválasztják a kettős spirál szálait. Harami Gábor, Gyimesi Máté, Ferencziová Veronika Ferencziová Veronika és a Motorenzimológiai Kutatócsoport további munkatársai és amerikai együttműködő kollégáik a DNS-helikázok összetett mozgási mintázatait fedezték fel, és Az USA Tudományos Akadémiájának lapjában (Proceedings of the National Academy of Sciences) közölt cikkkimutatták, hogy azok kulcsfontosságúak a nem megfelelő helyeken meginduló rekombináció megakadályozásában és ezáltal a káros génátrendeződések elkerülésében. Azt találták, hogy a helikázok a DNS-szálak mentén történő folyamatos mozgás helyett gyakran ún. ingázást (a DNS egyik száláról a másikra történő „átugrást” és ezzel járó irányváltást) végeznek, illetve előszeretettel bontják szét az olyan szerkezeteket, amelyekben egy DNS-szál egy másik, ép kettős spirál szálai közé támad.
Ezen aktivitások hiányában nagymértékben megemelkedik a „hibás” rekombináció valószínűsége, ami magasabb rendű szervezetekben, például emberben a rák gyakori okozója.
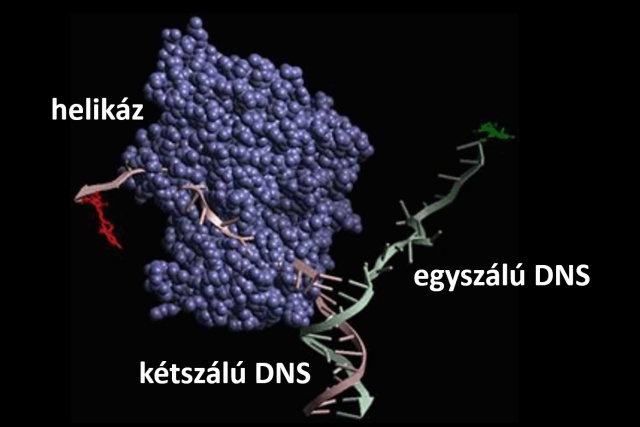 A helikáz motorenzimek a DNS két szálát választják szét, hogy azok információtartalma hozzáférhetővé és módosíthatóvá váljon
A helikáz motorenzimek a DNS két szálát választják szét, hogy azok információtartalma hozzáférhetővé és módosíthatóvá váljonÚj mechanizmusú antibakteriális szerek célpontja lehet egy DNS-karbantartó kölcsönhatásrendszer
A rekombináció minőség-ellenőrzését felderítő munka során Harami Gábor és kutatócsoportbeli társai ígéretes új kutatási irányt megalapozó felfedezéseket is tettek. Az ún. egyszálú DNS-kötő (single-stranded DNA binding, SSB) fehérjék minden élőlényben megtalálhatók: fő funkciójuk a DNS-anyagcsere (pl. megkettőződés, rekombináció) során megjelenő egyszálú DNS-szakaszok stabilizálása, védelme.
Emellett egy másik, kevésbé ismert, de hasonlóan életbevágó szerepet is játszanak: tucatnál több partnerfehérjével létesítenek kölcsönhatásokat, amelyek révén toborozzák („összehozzák”) a genomkarbantartó komplexeket. E kölcsönhatásokat a bakteriális SSB fehérjék kivétel nélkül egy rövid szakaszukon keresztül hozzák létre, amely szakasz – a nagyszámú partnernek való megfelelés kényszere miatt – rendkívül konzervált, és minden baktériumban nagyon hasonló szerkezetű. Ezért az olyan új hatóanyagok, amelyek ezen SSB-szakasz kölcsönhatásait gátolják, új mechanizmusú antibiotikumok ígéretes kiindulópontjául szolgálhatnak.
Az antibiotikum-rezisztencia korunk egyik legsúlyosabb egészségügyi problémája.
Az ilyen hatóanyagok előnye, hogy azokkal szemben – mivel egyszerre gátolnak egy egész kölcsönhatási hálózatot – a baktériumok a hagyományos (egy célpontos) szerekhez képest sokkal nehezebben tudnak rezisztenciát kialakítani.
Az említett SSB-kölcsönhatási mechanizmus eukariótákból (pl. emberből) teljesen hiányzik, az ezt gátló hatóanyagok tehát jó eséllyel nem okoznak majd nemkívánatos mellékhatásokat. A Motorenzimológiai Kutatócsoport a genomkarbantartó helikázok kutatásában kifejlesztett eszközökkel, illetve újszerű szűrőeljárásokkal kíván ilyen hatóanyagokat találni.
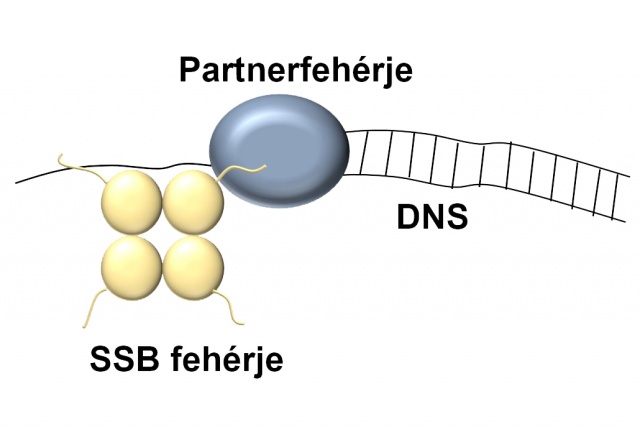 Az egyszálú DNS-kötő (SSB) fehérje (amely négy azonos egységből épül fel) DNS-kötő modulja (sárga golyók) mellett fehérje-fehérje kölcsönható szakaszt (sárga vonalak) tartalmaz, amelyen keresztül a DNS-hez toborozza a genomkarbantartást végző partnerfehérjéket (kék)
Az egyszálú DNS-kötő (SSB) fehérje (amely négy azonos egységből épül fel) DNS-kötő modulja (sárga golyók) mellett fehérje-fehérje kölcsönható szakaszt (sárga vonalak) tartalmaz, amelyen keresztül a DNS-hez toborozza a genomkarbantartást végző partnerfehérjéket (kék)További információ
Kovács Mihály
Telefon: +36-1-372-2500/8401




